马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册

x
https://www.liangyihui.net/doc/d ... mp;isappinstalled=1
% i. p! H, Y% F" t1 xBRAF在肺癌中的突变频率约为2-4%,是一个潜在的治疗靶点。一项全球多中心单臂临床试验证实,达拉非尼在经治或未经治疗的BRAF V600E突变的肺癌病人中具有抗肿瘤活性,总应答率为33%,中位无进展生存期为5.5个月。
" _. d1 J( z+ b1 ?1 r* ]+ M- O$ ^2 o3 i: l8 H+ v' k/ A# p
肺癌中的BRAF突变频率大约为2-4%,其中约一半为BRAF V600E突变。BRAF突变病人具有独特的临床病理特征:以吸烟人群为主,预后欠佳,对含铂化疗方案反应率低。达拉非尼(dabrafenib)是BRAF V600E突变的一个选择性强效抑制剂,已被批准用于不可切除或转移性突变黑色素瘤的治疗。达拉非尼用于BRAF突变的NSCLC治疗仅局限于一些个案报道或回顾性分析, Lancet Oncology最近在线发表了一项全球多中心单臂II期临床试验(NCT01336634)的结果。
: H2 J! D# \5 B0 ^. S
) p& f+ L0 i a2 [) j# _研究方案:- g' v" V2 s1 w" ]7 ]
1 O7 A0 I) K4 V+ n. r+ d
该研究是一项多中心、非随机、开放的II期临床试验的一部分(另外的两组病例用于评价达拉非尼+曲美替尼的安全性和疗效), 纳入了北美、欧洲和亚洲在内的10个国家的病例。入组病例为经治或未经治疗的IV期转移性BRAF V600E阳性的NSCLC,每天两次口服达拉非尼150mg。& w" R! T3 b7 p% P& Z7 h7 G
k6 P D- R5 v7 s7 c9 I% z; u主要结果:3 t1 i" m x) }# a7 E W
' c; _8 s. ` Q从2011年8月至2014年2月,共入组84例,其中有6例是接受达拉非尼为一线治疗方案。达拉非尼的中位治疗时间为4.6个月(IQR,1.8-11.1)。在78例经治的病例中,26例出现应答,总应答率为33%(见下图),中位无进展生存期(PFS)为5.5个月(95%CI, 2.8-6.9),中位总生存期(OS)为12·7 个月(95% CI , 7·3–16·9)。6例初治的病例中,有4例达到PR,他们的PFS分别为4·5, 8·6, 11·0和16·6个月。
5 C. M6 f* N | H# O
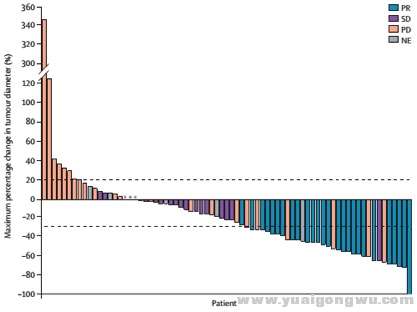
" \5 g3 i1 e/ A8 D- c9 Tsimon1.jpg! [: |# e' J& Q" N" a7 C k* Q o
; j+ }! f" `; a4 Y在治疗过中,45例(54%)出现了2级或以上的不良反应。最常见的3级或以上不良反应为皮肤鳞癌(12%)、基底细胞癌(5%)以及乏力(5%)。出现皮肤鳞癌的中位期是13.1周。有一位正在服用凝血因子Xa抑制剂的病例出现了颅内出血导致的死亡,并被认为是治疗药物相关的。3 L; e/ k7 m4 v6 w
' U& E" C! m- {7 i, H( T
研究结论:
y. q8 ]5 `& R& Q5 a( e. @' `# v& H- S n( }
达拉非尼在BRAF V600E突变的NSCLC中具有的抗肿瘤活性,可诱导持续的临床应答。达拉非尼可作为这个治疗手段有限的肺癌人群的一个治疗选择。; D, g, ?( F( e5 V' a* Q4 c
8 p) F" P/ @$ c7 A! j4 ?: q; C背景知识:; L% y6 s* d+ F1 i7 C9 \3 p
3 s$ H4 T, t8 G6 Q9 M- F: f6 s( J/ ORAS-RAF-MEK-ERK MAPK通路是最重要的经典癌症信号通路之一。BRAF是丝氨酸/苏氨酸激酶RAF家族的成员,结合到RAS并受其调控,直接活化MEK1/2,进一步磷酸化ERK1/2,见下图。BRAF突变可见于50%的黑色素瘤,45%的乳头状甲状腺癌,10%的结直肠癌和3%的肺癌。V600E突变的BRAF丝氨酸/苏氨酸结构域持续激活,可被达拉非尼和维罗非尼(vemurafenib)选择性抑制,两个药均已被批准黑色素瘤的治疗。3 c- I$ y7 g5 h/ B2 O
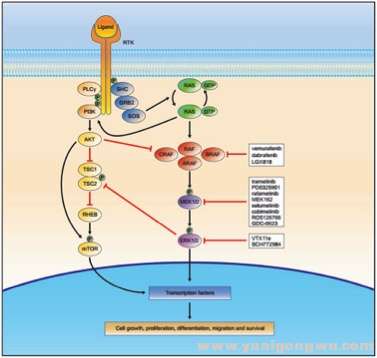
2 y6 p' A2 f8 i4 M- @2 |+ h3 W. ~. }simon2.jpg
3 W5 i! m4 I9 m, T2 s% K
% t' Z! T' W- X5 @- T9 {6 u# p(摘引自Nguyen-Ngoc等人. J Thorac Oncol.10)3 N0 y# b2 Q( M/ x
( k* U* O& O9 W3 n/ N1 p$ ?1 d
4 S; e% P. |. R: m B+ g$ n
( n, w H) {( ?+ o9 ~2 q
BRAF V600E抑制剂在NSCLC中的研究小结:7 ?( c7 J# {$ \6 p' J Y0 n
; H- Y$ b. u- n: A. g# }既往BRAF V600E抑制剂治疗突变NSCLC的研究多为个案报道,小编现把除本研究外的队列研究或前瞻性研究小结如下表:2 N8 K& h. T$ f) e* j6 q
8 c& b/ [& e' X# M. R( Zsimon3.png
9 x) k) A5 o7 r6 s& Z+ q$ p( t: G
9 f5 K0 O8 B3 W
8 s, P7 `3 S! g9 _/ o" J, d( s/ x3 d& g' D
LGX818是一个新型的BRAF抑制剂,NCT02109653试验是一个开放多中心单臂II期临床试验,评价其在化疗进展的BRAF V600E突变肺癌的安全性和疗效,但小编在ClinicalTrial.gov上查询后发现,该试验在开始前就撤回了注册。
6 ]4 m: q6 \) N/ R% C, P% M7 f6 U6 Y
5 B$ o( C# T2 X4 I* V3 K& n另外,MEK抑制剂曲美替尼、PD0325901和CI-1040均BRAF V600E或非V600E突变的NSCLC临床前模型中显现出了抗肿瘤活性。本临床试验的另一部分病例正是研究BRAF抑制剂和MEK抑制剂联用的安全性和临床疗效。
; S7 n5 y* B9 e; O6 \( a8 ?, G8 t
 0 x* w2 H1 _' ^, r9 n1 G- f$ z4 Z5 d
0 x* w2 H1 _' ^, r9 n1 G- f$ z4 Z5 d
1234.png
. T9 D H. g8 r5 e, x6 Z9 ?6 W# n b) T* b! ~. G. K; v' O
责任编辑:king
- d$ l" h0 n' |+ p; J# g, ]) y+ @: T& j- m1 g% G& T8 g1 ?2 Y
主要参考文献:9 J7 h7 m; C }& |* Y
9 F, T5 G2 i/ |/ X2 ?- RDabrafenib in patients with BRAFV600E-positive advanced non-small-cell lung cancer: a single-arm, multicentre, open-label, phase 2 trial. Lancet Oncology. 2016 Online
- [$ T) Q) f- M: y5 n3 X# ]2 j2 Y9 j) X- Z
BRAF Alterations as Therapeutic Targets in Non–Small-Cell Lung Cancer. J Thorac Oncol.2015 Oct. 10(10)
! L! a; b/ ?" P0 i' Z+ J$ j
# M$ {; W3 A2 X; QTargeted Therapy for Patients with BRAF-Mutant Lung Cancer. Results from the European EURAF Cohort. J Thorac Oncol.2015 Oct. 10(10)4 c) j3 c" {" M# {! a
. O4 y1 }: l: B. w f. t" o. x
VE-BASKET, a first-in-kind, phase II, histology-independent "basket" study of vemurafenib (VEM) in nonmelanoma solid tumors harboring BRAF V600 mutations (V600m). ASCO 20153 `: ~1 F1 c2 M0 W; w2 R/ R2 Y. [
5 E: f2 `# q* B4 _8 Y) q |