本文作者:Vv
1 S7 Z; [. T3 c% [3 l
1978年顺铂被正式获准使用,铂(Pt)作为抗癌药物进入临床,常见的铂类有:顺铂、卡铂、奈达铂、洛铂。
O5 ^0 a) l# Y# p
40多年后,即使在精准医学、靶向、免疫疗法时代的冲击下,铂类药物依然是使用最广泛的抗癌药物之一。
3 c) Q8 G: j8 q! Q4 sDNA损伤修复功能异常是肿瘤发生发展的重要特点之一,在癌症发展过程中,大多数癌症失去了关键的DDR途径,DNA损伤反应(DDR)为Pt药物敏感性提供了解释。
$ ]( ?3 [$ `$ d/ n# U8 q铂类药物共同的细胞杀伤作用机理:他们可与DNA双链中的嘌呤碱基共价结合,这种共价结合使得DNA双链形成固定的构型,从而产生DNA双链局部变性,若这种损伤不能被有效修复,细胞会通过凋亡或非凋亡途径死亡。
3 h- i% ~5 k' [ X% k1 `2 W
但与此同时,铂类治疗所带来的毒副作用如:脊髓毒性、恶心呕吐、腹泻、肝肾毒性和神经毒性等等,让患者苦不堪言,有些副作用甚至在停药后,也不可逆转。
* c5 T; Q. u) vPt药物发展史
0 r5 c8 l9 i/ Z; u
正如标题所示,今天的主角是人类最广泛应用的化疗药物之一——“卡铂。
; F& T9 Q( ]- \: P. f( B! e
由于铂类药物是细胞周期非特异性药物,可作用于细胞增生周期的各个时相,对肿瘤细胞的作用强而快,能迅速杀灭癌细胞,其剂量反应曲线接近直线,在体内能耐受的毒性限度内,其杀伤能力随剂量增加而提高,血药浓度是影响疗效的最主要因素。
! w) T" G" R4 ^# O* I( `通常情况下,在患者耐受的情况下,要尽可能的把使用剂量提高。
% @2 H& b. @9 e' M# F如今,这位抗癌药中的老干部也开花了,最新的一则来自《Cancer Letters》期刊的研究综述“小剂量“卡铂”通过STING信号通路重组肿瘤免疫微环境并与PD-1抑制剂协同治疗肺癌”——铂类Pt,也搭上了免疫联合疗法春天的列车。
7 y* n. V+ h1 M. j2 h接下来,Vv就给大家讲讲这条新闻到底怎回事~
9 S2 y4 Z! Y3 Q3 K4 G
! l4 }0 i$ }6 ~1 Q) v A* T
免疫联合疗法在肺癌领域中一直是一个热点,但是真正关于协同作用机制的研究却非常少,安全性也是临床医生在联合治疗选择时所考虑的重要问题,因此,确定合理的化疗剂量和化疗周期,探讨其与免疫治疗的协同作用机制,具有重要意义。
8 Y1 A' E$ J" J0 {0 E# E& X' a这项研究发现“卡铂”可以诱导DNA损伤,激活经典的STING/TBK1/IRF3通路和非经典的STING-NF-κB信号复合物。低剂量卡铂通过信号核心STING,将“冷”肿瘤变为“热”肿瘤,增加CD8+T细胞浸润,增加PD-L1表达,从而增强PD-1抑制剂的抗肿瘤作用;
. `' _0 F9 ^% W( W5 d
重要的是,没有副作用。
, ` R; O9 v1 d! U此外,阻断肿瘤细胞的STING可有效逆转PD-L1的上调和STING通路的激活,降低卡铂和卡铂-PD-1抑制剂联合应用的抗肿瘤作用。
( ~' v5 f& \) p. z我们的研究结果共同报道了低剂量卡铂靶向在STING通路中的作用,为提高PD-1抑制剂治疗肺癌的疗效提供了一个经济、有效和安全的选择。
+ B: _$ I5 E/ d- F" F
7 V+ G3 E' T3 F( G/ L S, }, G/ L3 ~8 g( N3 {
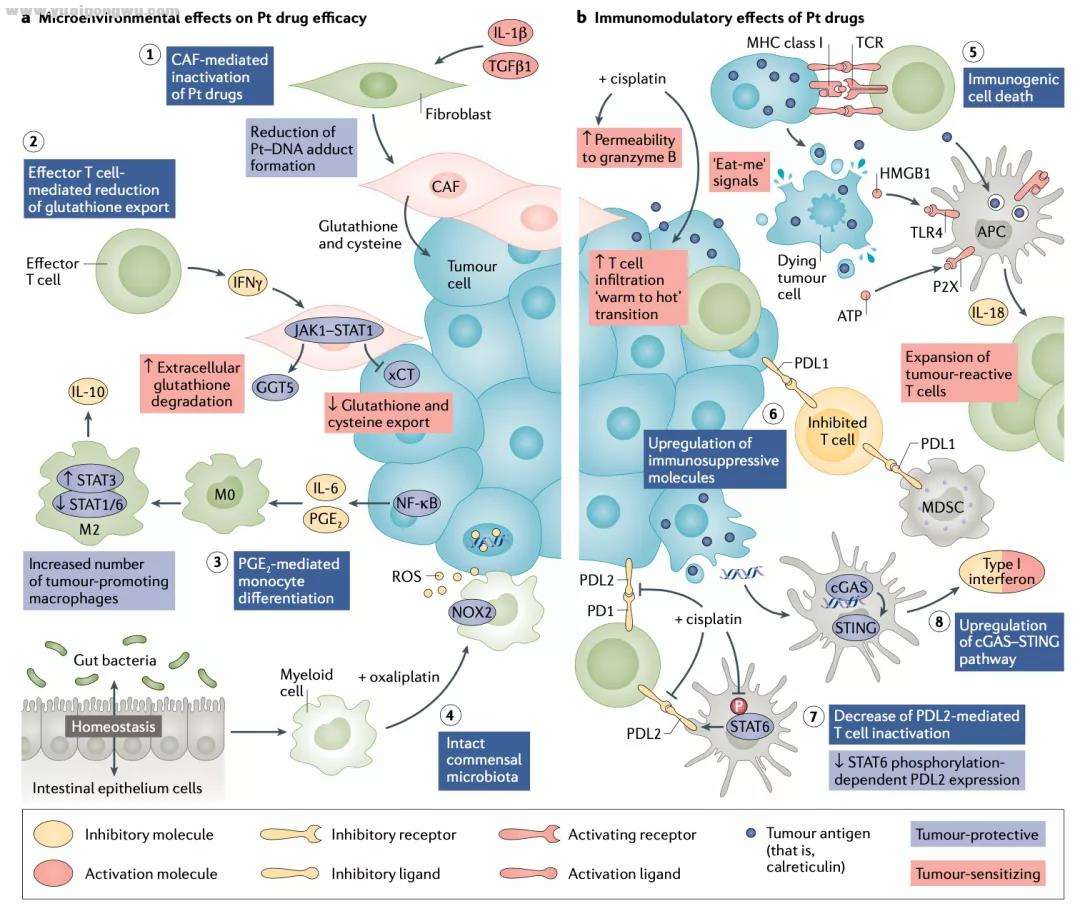
铂类药物和肿瘤微环境相互影响,Pt化合物对肿瘤微环境表现出了免疫调节作用,Pt治疗增加了肿瘤新抗原的释放,导致肿瘤反应性细胞通过受刺激,抗原呈递细胞分泌扩大。
# M, ?6 S! J; Q0 ?# `
在以往的研究综述中也曾经报道过““顺铂”可增加NSCLC(非小细胞肺癌)STING通路的激活和PDL1表达” 在治疗初期和复发的肺腺癌中,STING激活与较高水平的内源性DNA损伤、靶向免疫检查点和趋化因子有关。
+ v" `% p! d* e& s1 h" M临床观察到,较高频率的(STK11)突变具有较低STING和免疫表达;而TP53共突变的肿瘤中,则显示出较高的免疫和STING相关基因表达。
1 I) v" q/ m& S
NSCLC中STING通路的激活可预测免疫治疗反应的特征,顺铂治疗可增加多个NSCLC临床前样本(包括腺癌和鳞癌)中STING通路的激活和PD-L1的表达。
4 d! {4 R0 M. @3 o
以上内容没听懂的小伙伴可以跳过,Vv来帮你直接抓重点:
1. 铂类对肿瘤微环境有调节作用
2. 低剂量卡铂增加CD8+T细胞浸润和PD-L1表达。
3. 低剂量的卡铂是安全的,可以把“冷”的肿瘤变成“热”的肿瘤。
4. 小剂量卡铂增强PD-1抑制剂的抗肿瘤作用。
5. 卡铂诱导DNA损伤并激活STING信号通路。
6. 在肿瘤中抑制STING可逆转低剂量卡铂的抗肿瘤作用。
% e1 F( v U* P W# Q1 h6 Z最后,Vv提醒大家,虽然“铂类”老树开花为我们的免疫联合疗法,又开辟了全新的“减法”思路,但基于目前关于单药低剂量铂类联合免疫的研究,仍存在缺陷,临床证据仍不够充分,我们并没有大规模临床对比实验证明,这种联合疗法在生存期和疗效上明显优于免疫单药或其他免疫联合疗法,具体到实际应用中还需要尊重医嘱哦~
) R% F% [/ k/ q. F* a* O! Y
小伙伴们,今天你学会了吗?
0 H% y3 G" g1 M9 _( o
6 Q# c6 X) t$ \- A# s2 n- ^6 ]" L* H7 `! y1 H4 ~% }
* i# }9 z8 I; f# d) z9 Y