马дёҠжіЁеҶҢпјҢз»“дәӨжӣҙеӨҡеҘҪеҸӢпјҢдә«з”ЁжӣҙеӨҡеҠҹиғҪпјҢи®©дҪ иҪ»жқҫзҺ©иҪ¬зӨҫеҢәгҖӮ
жӮЁйңҖиҰҒ зҷ»еҪ• жүҚеҸҜд»ҘдёӢиҪҪжҲ–жҹҘзңӢпјҢжІЎжңүиҙҰеҸ·пјҹз«ӢеҚіжіЁеҶҢ

x
жң¬её–жңҖеҗҺз”ұ Emj дәҺ 2020-1-4 09:56 зј–иҫ‘
# t5 @- _. N4 y S2 `8 M/ W7 |) ~, K4 P( b: j4 {4 A
йҡҸзқҖеҢ»еӯҰзҡ„дёҚж–ӯеҸ‘еұ•пјҢе®һдҪ“зҳӨз–—ж•ҲиҜ„дј°д№ҹйҡҸд№ӢеҸҳиҝҒпјҢд»Һ1981е№ҙйҰ–ж¬ЎеҸ‘иЎЁзҡ„WHOпјҢ2000е№ҙRECISTпјҢ2009е№ҙе…Қз–«ж—¶д»Јзӣёе…із–—ж•ҲirRCпјҢзӣҙеҲ°дјҙйҡҸзқҖе…Қз–«жЈҖжҹҘзӮ№жҠ‘еҲ¶еүӮзҡ„йЈһйҖҹеҸ‘еұ•пјҢ2017е№ҙжӣҙз¬ҰеҗҲдёҙеәҠе®һи·өзҡ„иҜ„дј°ж ҮеҮҶ:iRECISTиҜһз”ҹпјҢдҪҝеҫ—жӣҙеӨҡжӮЈиҖ…еңЁйҖҗжёҗе®Ңе–„зҡ„иҜ„дј°ж ҮеҮҶдёӢиҺ·еҫ—OS收зӣҠгҖӮ
1 y, g( _2 ^! h& N5 r жҺҘдёӢжқҘпјҢVvеёҰдҪ ж•ІйҮҚзӮ№пјҢиҪ»жқҫе®һз”Ёзҡ„жҺҢжҸЎе…Қз–«жІ»з–—иҝҮзЁӢдёӯзҡ„iRECISTгҖӮ' }! l6 a3 [# \9 P0 w
1. RECIST
/ W8 A+ h" j% ^ A' P" L& A RECISTжҳҜз”ұдёҙеәҠз ”з©¶иҖ…гҖҒеҲ¶иҚҜиЎҢдёҡгҖҒеҪұеғҸеӯҰ专家гҖҒзҫҺеӣҪеӣҪз«ӢзҷҢз—Үз ”з©¶жүҖ(NCI)гҖҒеҠ жӢҝеӨ§еӣҪз«ӢзҷҢз—Үз ”з©¶жүҖ(NCIC)гҖҒиӢұеӣҪзҷҢз—Үз ”з©¶зҪ‘з»ң(NCRN)гҖҒ欧жҙІзҷҢз—Үз ”з©¶е’ҢжІ»з–—з»„з»Ү(EORTC)е…ұеҗҢеҲ¶е®ҡпјҢдё»иҰҒй’ҲеҜ№е®һдҪ“зҳӨзҡ„з–—ж•ҲиҜ„д»·зҡ„ж ҮеҮҶгҖӮ(йқһе®һдҪ“зҳӨдёҚйҖӮз”ЁпјҢеҰӮиЎҖж¶І), {& g1 n7 a2 I$ W0 j. Q
2.е®һдҪ“зҳӨжөӢйҮҸж–№жі•пјҡеҚ•еҫ„жөӢйҮҸжі•
9 H! c! f6 p+ W' Z/ r' J иҮіе°‘жңүдёҖжқЎеҸҜд»ҘеҮҶзЎ®жөӢйҮҸзҡ„зӣҙеҫ„пјҲи®°еҪ•дёәжңҖеӨ§еҫ„пјүгҖӮ
+ ]# f1 Q2 z3 N; D
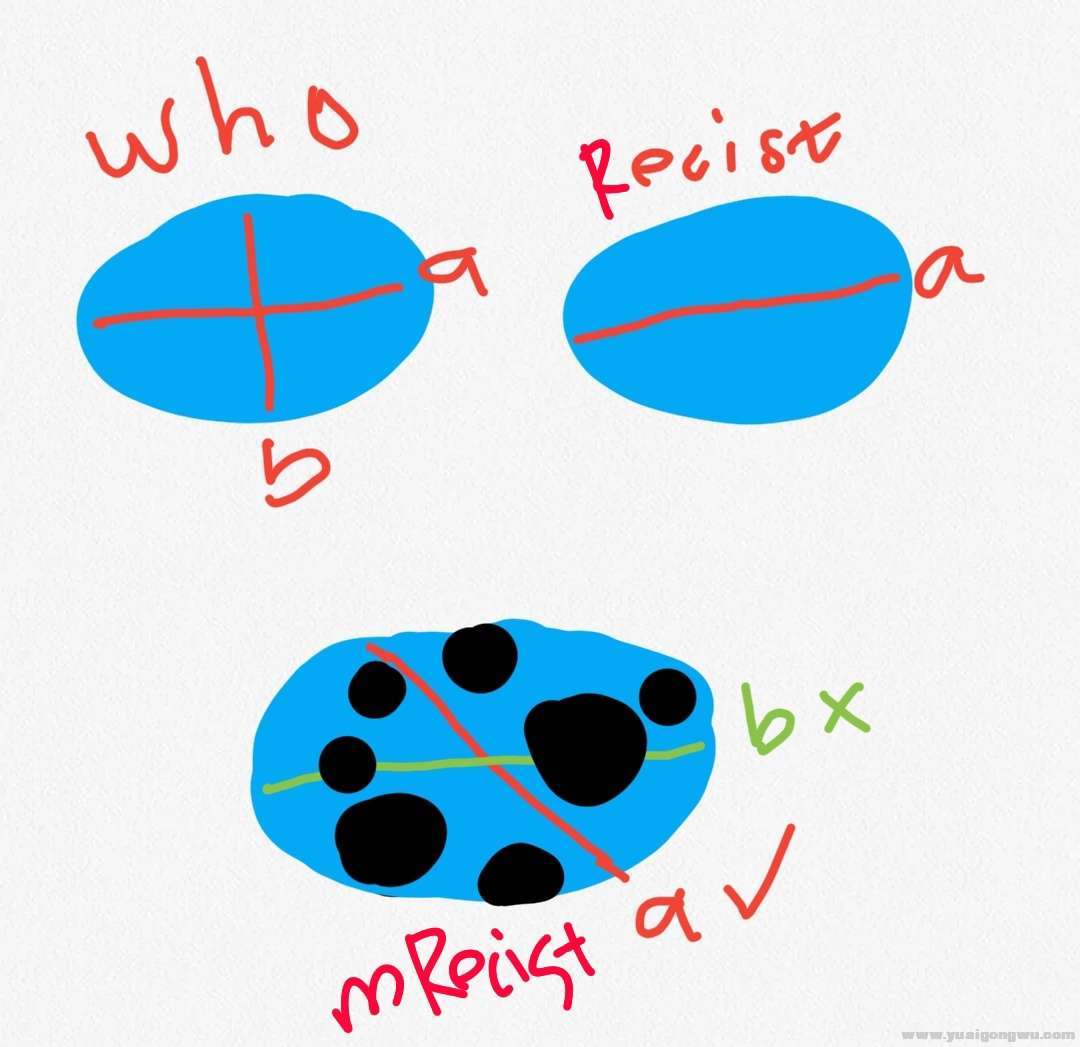 ) d5 t9 z u* S0 ?/ L
) d5 t9 z u* S0 ?/ L
иӮҝзҳӨзҡ„зӣҙеҫ„(RECIST)еҸҳеҢ–еҸҜиҫғеҸҢеҫ„д№ҳз§Ҝ(WHO)зҡ„еҸҳеҢ–жӣҙеҘҪзҡ„еҸҚжҳ иӮҝзҳӨз»Ҷиғһзҡ„еҸҳеҢ–пјҢйҮҚеӨҚж•ҲжһңеҘҪпјҢеҮҸе°‘иҜҜе·®гҖӮmRECISTд»ҘвҖңеӯҳжҙ»иӮҝзҳӨвҖқдҪңдёәиҜ„дј°еҜ№иұЎпјҲжҺ’йҷӨеқҸжӯ»иӮҝзҳӨзҡ„е№Іжү°пјүгҖӮ) n) ]4 B# w1 R' `7 a3 |' u
жіЁ:е…Қз–«жІ»з–—иҝҮзЁӢдёӯпјҢжІ»з–—жңүж•ҲпјҢз—…зҒ¶еёёе‘ҲзҺ°еҸҳи–„пјҢеҸҳж·ЎпјҢдёӯеӨ®й•Ӯз©әпјҢеҶ…йғЁз“Ұи§ЈиҮідёҚеҸҜжөӢйҮҸзҡ„еҪұеғҸзү№еҫҒгҖӮ+ S% `$ W. R0 e2 O3 ]
3.еҸҜжөӢйҮҸз—…зҒ¶
5 Z. I/ q, x. W' M$ l е®ғиҮіе°‘еңЁжөӢйҮҸе№ійқўдёҠзҡ„дёҖдёӘзӣҙеҫ„зәҝдёҠиғҪеӨҹиў«еҮҶзЎ®жөӢйҮҸ并记еҪ•гҖӮ8 Q' X2 P, y9 J
еҸҜжөӢйҮҸйқһж·Ӣе·ҙз»“иӮҝзҳӨз—…зҒ¶пјҡжөӢйҮҸжңҖй•ҝзӣҙеҫ„гҖӮ
6 i% W2 t$ \ s& [: P! aеҸҜжөӢйҮҸжҒ¶жҖ§ж·Ӣе·ҙз»“пјҡ жөӢйҮҸжңҖзҹӯзӣҙеҫ„гҖӮ9 `7 i4 s. x, F0 _( g9 s
4.дёҚеҸҜжөӢйҮҸз—…зҒ¶
" L/ \: z Y" h* e з—…зҗҶжҖ§ж·Ӣе·ҙз»“:жңҖзҹӯзӣҙеҫ„вүҘ10mmдё”пјң15mmгҖӮ
7 S' b; h' u* O7 A1 k! U йқһж·Ӣе·ҙз»“:CTжү«жҸҸжңҖй•ҝзӣҙеҫ„пјң10mmгҖӮ- d5 _7 g9 m: `9 | E
жіЁ:иҪ»йӘЁй«“зӮҺгҖҒи„‘иҶңз—…еҸҳгҖҒи…№и…”з§Ҝж¶ІгҖҒиғёи…”з§Ҝж¶ІгҖҒеҝғеҢ…з§Ҝж¶ІгҖҒзӮҺжҖ§д№іи…әз—…гҖҒзҡ®иӮӨжҲ–иӮәзҡ„зҷҢжҖ§ж·Ӣе·ҙз®ЎзӮҺгҖҒи…№йғЁиӮҝеқ—/и…№и…”еҷЁе®ҳиӮҝеӨ§зӯүпјҢеҪұеғҸеӯҰдёҚиғҪиў«жөӢйҮҸйңҖйҖҡиҝҮзү©зҗҶжЈҖжҹҘзЎ®е®ҡзҡ„з—…зҒ¶д№ҹжҳҜдёҚеҸҜжөӢйҮҸз—…зҒ¶гҖӮ
7 K8 Z+ ^) d5 K8 `) w4 P5. iRECIST( R. r) }0 y, N% @$ |
iRECISTпјҲmodified RECIST1.1 for immune based therapeutics, iRECIST3 |. W1 O( L9 d7 R! g% L
iRECISTеј•е…ҘдәҶiUPDжҰӮеҝөпјҲеҫ…иҜҒе®һзҡ„з–ҫз—…иҝӣеұ•пјүпјҢеҠЁжҖҒиҜ„дј°е…Қз–«жІ»з–—иҝҮзЁӢдёӯеҸҜиғҪеҮәзҺ°зҡ„йқһе…ёеһӢжЁЎејҸгҖӮеӣ жӯӨпјҢеҸӘиҰҒжӮЈиҖ…дёҙеәҠзЁіе®ҡжғ…еҶөдёӢпјҢеӨ„ж–№еҢ»з”ҹеңЁеҲӨж–ӯiUPDеҗҺд»Қ继з»ӯзҺ°жңүзҡ„жІ»з–—гҖӮ
# W* H5 h' x @( fеҫ…иҜҒе®һзҡ„з–ҫз—…иҝӣеұ•(PDйңҖиҰҒиў«иҜҒе®һ)
0 ^( z1 y& j% u( T% y& ~8 h" pеҫ…иҜҒе®һ:
% X" q- o' G! d4 d" j; T, eз—…зҒ¶иҝӣеұ•жҲ–еҮәзҺ°ж–°з—…зҒ¶з¬ҰеҗҲiRECIST)вҶ’IUPD
( T! k9 a$ G$ ?+ c1 ~7 I IUPDз¬ҰеҗҲiRECISTвҶ’iSD/iPR/iCR
5 z+ y) l" T7 B& KзЎ®и®Ө:
, |, Z, M5 s/ k2 y( W, V# h6 DеҺҹIUPDиҝӣдёҖжӯҘжҒ¶еҢ–вҶ’PD) Z6 w v- O- e, E
жңӘIUPDз—…зҒ¶з¬ҰеҗҲRECIST1.1иҝӣеұ•вҶ’PD
& U3 t8 W0 [( L% Z1 S% V3 L
% l( z5 ^* ]% R" D( |/ H E. s' c) ~
t# P; R" h4 r) x, \9 e( O9 v: G) E! j& m V9 y; r0 C8 X
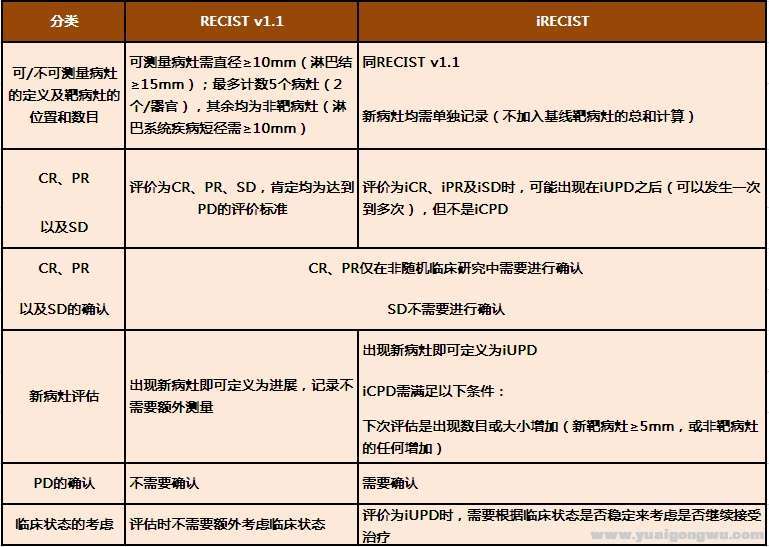 + ^7 j3 c4 c( G# W5 t; r
+ ^7 j3 c4 c( G# W5 t; r
жіЁ:дёҙеәҠзҠ¶жҖҒзЁіе®ҡзҡ„иҜ„дј°ж–№ејҸпјҡ
* k' l7 K3 C7 C0 U* B5 V" f) K! }1гҖҒжӮЈиҖ…дҪ“еҠӣжҙ»еҠЁзҠ¶жҖҒпјҲPSпјүиҜ„еҲҶжІЎжңүдёӢйҷҚ% D+ a ?, l3 x; F$ g5 f! u( @+ j
2гҖҒз–ҫз—…зӣёе…із—ҮзҠ¶жІЎжңүеҠ йҮҚпјҡеҰӮз–јз—ӣгҖҒе‘јеҗёеӣ°йҡҫ
1 B3 `) b4 K, X3 \/ @5 \+ s2 D3гҖҒж— йңҖеўһеҠ з–ҫз—…зӣёе…із—ҮзҠ¶зҡ„жІ»з–—жҺӘж–ҪгҖӮ
1 H# `* R, s* b A# c6.йқһе…ёеһӢзј“и§ЈжЁЎејҸ
3 K* {! q- Q( o; dдё»иҰҒиЎЁзҺ°дёә:延иҝҹеә”зӯ” еҒҮжҖ§иҝӣеұ• еҲҶзҰ»еҸҚеә”
# W. w t @7 M4 }% H: ]( zдёҖйЎ№PD1/ PDL1жҠ‘еҲ¶еүӮжІ»з–—иҪ¬з§»жҖ§NSCLCзҡ„дёҙеәҠз ”з©¶(n=160)жҳҫзӨәпјҢеңЁжҺҘеҸ—е…Қз–«жІ»з–—зҡ„жӮЈиҖ…дёӯ13%зҡ„жӮЈиҖ…еҸ‘з”ҹйқһе…ёеһӢзј“и§ЈжЁЎејҸпјҢе…¶дёӯ8дҫӢдёәеҒҮжҖ§иҝӣеұ•пјҢRECIST1.1дҪҺдј°дәҶ11%е®һйҷ…жІ»з–—жңүж•Ҳзҡ„жӮЈиҖ…гҖӮ/ w% H# o7 p; c: a6 R
- O; b/ l/ T4 M
/ }& A$ [9 m. M/ ]
 a- M" L+ G1 \% a2 X8 z
a- M" L+ G1 \% a2 X8 z
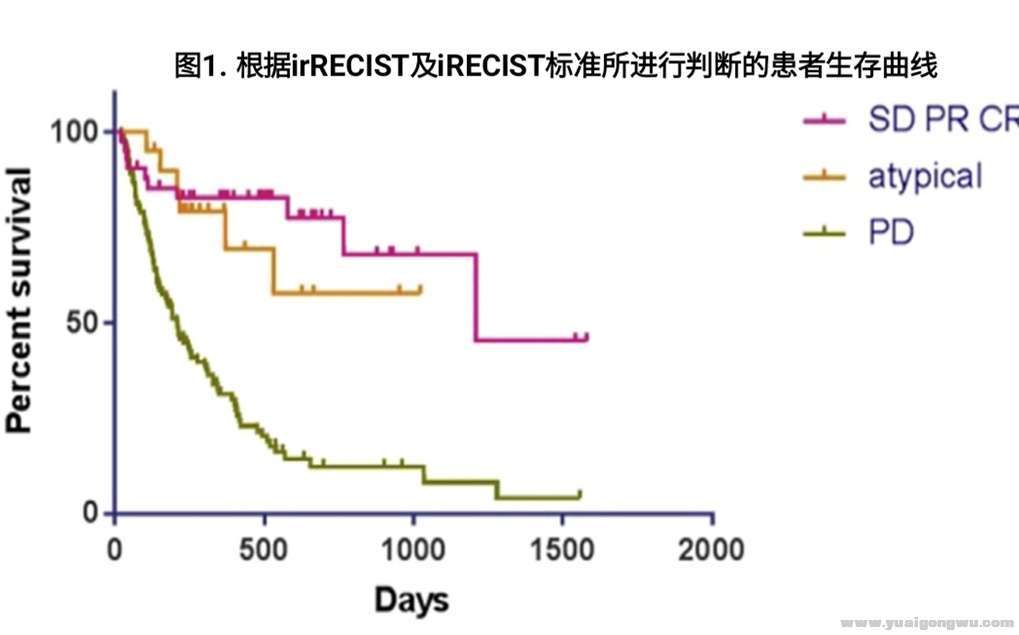 9 A( s! `" s4 [9 q( k2 o! k# N5 I
9 A( s! `" s4 [9 q( k2 o! k# N5 I
7.з–ҫз—…иҝӣеұ•еҗҺ继з»ӯжІ»з–—TBP(жңүдәүи®®)" g3 B/ k g# A% g5 d! z
жҢүз…§RECISTиҜ„дј°пјҢIOжІ»з–—ж— ж•ҲжҲ–иҖҗиҚҜеҗҺпјҢжӮЈиҖ…жңӘеҮәзҺ°з–ҫз—…еҝ«йҖҹиҝӣеұ•пјҢеҜ№е…Қз–«жІ»з–—жңүиүҜеҘҪзҡ„иҖҗеҸ—жҖ§пјҢ继з»ӯдҪҝз”ЁпјҢд»Қжңү19%зҡ„жӮЈиҖ…еҸҜиғҪжңүж•ҲпјҢеҸҜ延й•ҝдёҖеҖҚзҡ„з”ҹеӯҳжңҹ24.4дёӘжңҲvs11.2дёӘжңҲ(еҪ»еә•ж”ҫејғе…Қз–«жІ»з–—)
* k$ x% C; J7 X- E/ O! o
- a' W, [5 B0 g8 V/ g4 B
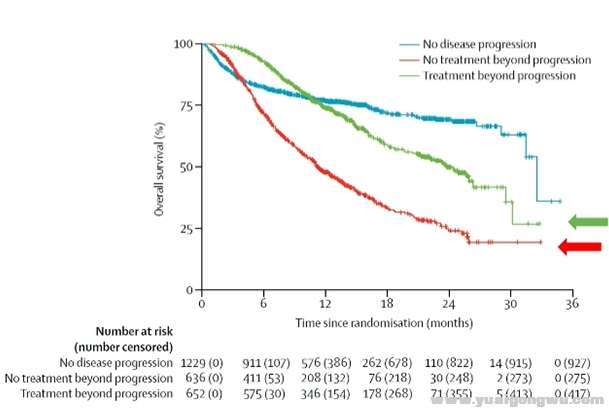 ! q* {- q, |, H
! q* {- q, |, H
8.и¶…иҝӣеұ•; i4 {6 Y/ ~8 F7 Q- H
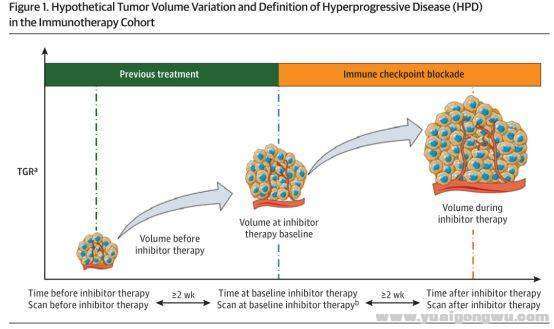
жҺҘеҸ—е…Қз–«жІ»з–—еҗҺпјҢиӮҝзҳӨеҸҚеёёеҠ йҖҹз”ҹй•ҝпјҢз—…жғ…жҖҘеү§жҒ¶еҢ–пјҢиҝҷз§ҚзҺ°иұЎз§°дёәи¶…иҝӣеұ•пјҲHyperprogression DiseaseпјҢHPDпјүгҖӮ
, t+ o0 ]. y/ n# Q5 y4 oHPDеә”жңүдёҘж јзҡ„ж—¶й—ҙзӘ—еҸЈе’ҢиҜ„дј°з•Ңе®ҡ:
8 K8 [" v9 u3 r! Z9 UпјҲ1пјүеңЁе…Қз–«жЈҖжҹҘзӮ№жҠ‘еҲ¶еүӮжІ»з–—еҗҺ第дёҖж¬ЎиҜ„д»·ж—¶иҝӣеұ•пјҢиҮіжІ»з–—еӨұиҙҘж—¶й—ҙпјҲTTFпјүп№Ө2жңҲпјӣ* x# d( [. E/ x
пјҲ2пјүиӮҝзҳӨдҪ“з§ҜеўһеҠ >50%пјӣ
F- O) t1 c/ wпјҲ3пјүиӮҝзҳӨеўһй•ҝйҖҹеәҰпјҲTGRпјүеўһеҠ >2еҖҚгҖӮ
9 x2 y" s( R# B0 @! G' c) c. WиӢҘеҮәзҺ°HPDз—ҮзҠ¶пјҢе»әи®®е°Ҫж—©иҖғиҷ‘з”ұе…Қз–«з–—жі•иҪ¬еҗ‘жҠўж•‘еҢ–з–—гҖӮ
5 ~( m4 n* d% E1 T$ ~ U2 w) [
 5 y+ [ p/ q! Z1 L9 e
5 y+ [ p/ q! Z1 L9 e
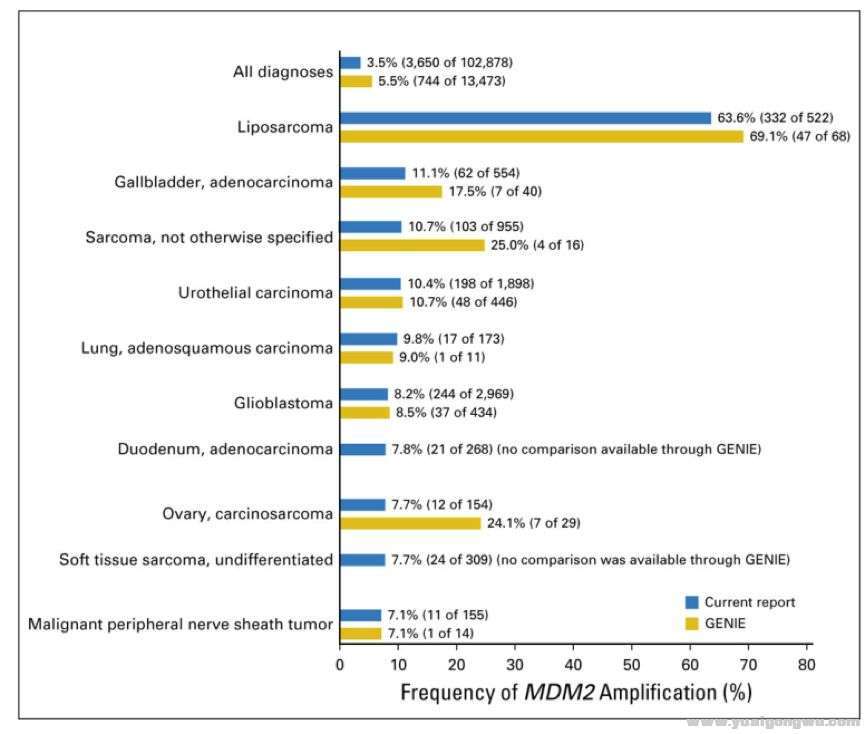
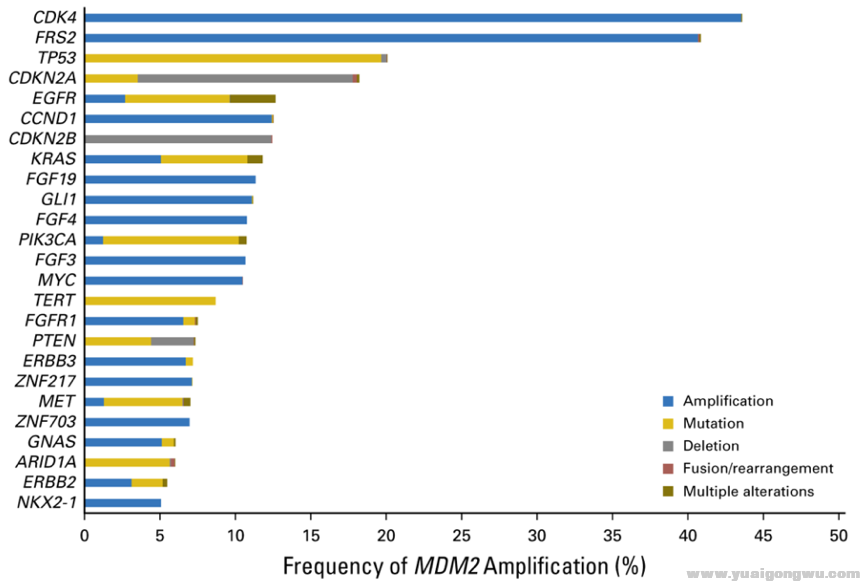
9. MDM2/ MDM4жү©еўһдёҺи¶…иҝӣеұ•зӣёе…іжҖ§$ f/ O7 M! i0 f; O+ N Q
2017е№ҙ3жңҲпјҢKatoзӯүеңЁCCRдёҠжҠҘйҒ“дәҶеңЁ155дҪҚиӮҝзҳӨжӮЈиҖ…дёӯпјҢз»Ҹе…Қз–«иҚҜзү©жІ»з–—еҗҺпјҢTTFпјҲtime to treatment failureпјү<2дёӘжңҲзҡ„6дҪҚжӮЈиҖ…пјҲеқҮдёәжҺҘеҸ—PD-1/PD-L1жҠ‘еҲ¶еүӮжІ»з–—зҡ„жӮЈиҖ…пјүпјҢйғҪе…·жңүMDM2/MDM4жү©еўһгҖӮ, x h, h, b2 @* m
2019зҫҺеӣҪдёҙеәҠиӮҝзҳӨеӯҰдјҡпјҲASCOпјүе№ҙдјҡзҡ„ж‘ҳиҰҒдёӯпјҢдёҖйЎ№йқһе°Ҹз»ҶиғһиӮәзҷҢпјҲNSCLCпјүеӣһйЎҫжҖ§з ”究еҲҶжһҗдәҶ20дҫӢдёҖзәҝеё•еҚҡеҲ©зҸ еҚ•жҠ—жІ»з–—зҡ„жҷҡжңҹжӮЈиҖ…пјҢе…¶дёӯ5дҫӢжӮЈиҖ…еҮәзҺ°дәҶHPDпјҢз ”з©¶иҖ…йҖҡиҝҮиҚ§е…үеҺҹдҪҚжқӮдәӨжҠҖжңҜпјҲFISHпјү гҖҒе…Қз–«з»„еҢ–пјҲIHCпјүе’ҢNGSеҲҶжһҗпјҲFoundationOne CDxпјҢFMIпјүжҳҫзӨәпјҢ5дҫӢHPDжӮЈиҖ…еқҮеӯҳеңЁMDM2жү©еўһгҖӮ8 P& P: i" W& M4 R
жіЁпјҡCDKN2A/Bеҹәеӣ зјәеӨұеҸҠMDM2ж”№еҸҳдёҺе…Қз–«HPDеҜҶеҲҮзӣёе…ігҖӮ
! f' {4 \3 H# j
. O8 W( S6 c! v
5 u8 A' d m. c, C: `/ ~е…Қз–«жІ»з–—д»ҚеӨ„дәҺжҺўзҙўпјҢж•ҙзҗҶпјҢеҸҚжҖқзҡ„йҳ¶ж®өпјҢеҫҲеӨҡи®әиҜҒе’Ңи§ӮзӮ№д№ҹеҫ…йҡҸд№Ӣж”№йқ©пјҢиҝӣеҢ–пјҢйҖҗжӯҘе®Ңе–„гҖӮ
+ O& o7 ~3 W8 ^еёҢжңӣVvдёҺеӨ§е®¶еңЁеӯҰд№ жҺўзҙўзҡ„йҒ“и·ҜдёҠпјҢ并иӮ©дҪңжҲҳгҖӮ
: I9 e/ D5 u* h! G Q
 4 k8 O7 d) ?# h5 _% ]' G
4 k8 O7 d) ?# h5 _% ]' G
|


