马上注册,结交更多好友,享用更多功能,让你轻松玩转社区。
您需要 登录 才可以下载或查看,没有账号?立即注册


x
本帖最后由 青菜567 于 2026-1-13 10:57 编辑
整理:淡然清欢、年去岁来、张帆、雨过天晴 审核:张蕻梅、钱哲、鹰版 由于肺癌异质性强、病情复杂,单一学科的治疗模式难以全面覆盖患者的需求。多学科诊疗(MDT)模式正是打破学科壁垒的关键——通过肿瘤内科、胸外科、病理科、影像科、放疗科等多领域专家的联合研判,能够为患者提供更精准的诊断、更个性化的治疗方案。
6月15日,来自北京胸科医院的多位权威专家再次齐聚云端,开启“肺常守护,MDT云端护航行动”第三期活动,继续以深厚的临床经验和前沿的学术视角,深入分析典型病例,探讨诊疗难点,为患者点亮希望之光。在这篇科普文章中,小编精心梳理了第三期直播活动中的全程精华观点,以期让更多患者获益。
点击文末左下角【阅读原文】可观看直播回放。
主持人 钱 哲 教授 北京胸科医院肿瘤中心 讨论专家: 林 根 教授 北京胸科医院肿瘤中心 唐俊舫 教授 北京胸科医院肿瘤中心 张 旭 教授 北京胸科医院放疗科 贺 伟 教授 北京胸科医院影像科 杨 志 教授 北京胸科医院胸外科
病例一:肉瘤样癌靶向策略及局部治疗探讨





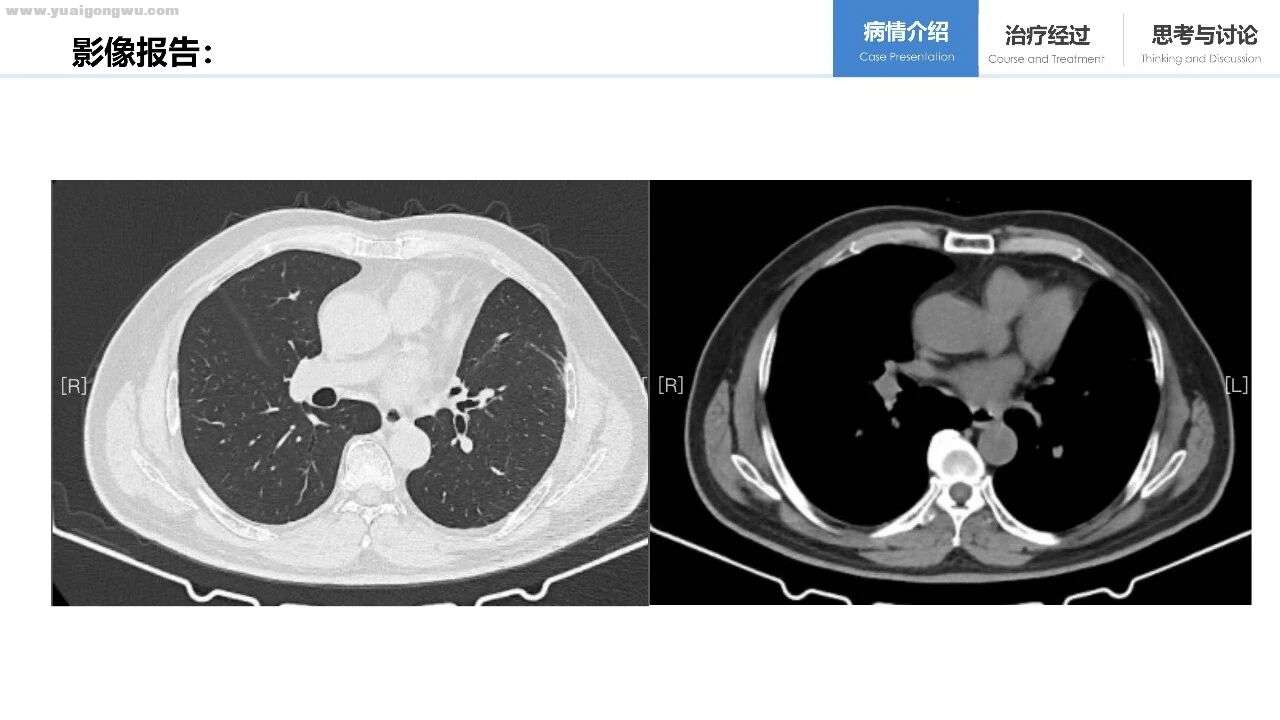








患者诉求: 1、患者一线治疗入组靶向药,2月余耐药;二线免疫+抗血管,至今半年余,期间左侧肾上腺病灶稳中有缩,右侧肾上腺病灶二线治疗4个月后出现局部进展,进行了消融处理,术中穿刺取了组织,但由于有效样本量太少仅找到癌细胞,未给出病理类型,无法做基因检测。患者近期药物副作用逐渐出现,主要为皮疹、口腔疼痛、鼻出血等,越来越难以耐受。尚未进行化疗、放疗等手段治疗。希望能够得到下一步的治疗指导。
2、如仍然取不到病理组织,二线方案耐药或副作用不耐受后该何去何从?适合放疗吗?体外还是粒子?早点开始放疗好,还是疾病进展后再放?
3、放疗和消融如何选择?化疗药物的选择?是否有后线适合的临床试验?是否还有根治的可能?
贺伟教授 从提供的影像资料来看,患者初期病变呈现片状或块状形态,两个月后描述为肿块。结合PET-CT检查结果,考虑病变为炎症伴出血,提示存在代谢活性,且周围可能伴有磨玻璃密度改变。目前可确定为肿瘤,肿瘤周围的磨玻璃影可能由出血、感染或肺组织肿瘤浸润所致。
从术后改变观察,未见侵及肺膜。八个月后病变出现厚壁空洞,与前期无空洞的病变表现不同。回顾患者首次CT影像,可见病变密度不均匀,内部存在坏死区域,推测可能是坏死组织排出后形成厚壁空洞。
在影像鉴别方面,肉瘤与常规肺癌较难区分。肉瘤好发于胸膜下区域,以上肺多见,部分病例可出现坏死。但仅凭借影像学表现,尚无法直接确诊为肉瘤样癌。此外,患者纵隔淋巴结无肿大,肾上腺病变内部坏死较多,其他方面未见特殊异常。治疗方案的制定需结合临床综合考量。
唐俊舫教授 肉瘤样癌在临床上发病率相对较低,其常见基因突变包括MET14号外显子跳跃突变,以及KRAS G12C驱动基因突变。该患者初诊时已属IV期(存在远处孤立转移),虽接受肺根治术,但因肾上腺转移灶与周围组织粘连紧密,未能完成肾上腺转移灶手术切除。
针对此类情况,若初次根治术未达治疗目标,是否可通过立体定向放射治疗(SBRT)等精准局部放疗,或射频消融等局部治疗手段,实现更长时间的疾病控制?该患者因无法手术而使用了针对KRAS G12C突变的靶向药物JAB-21822(此药于2025年第二季度刚上市,患者应是参加了临床研究)。临床研究显示,该药物对KRAS G12C突变患者有效率较高,但该患者无进展生存期(PFS)不足3个月(仅2个多月)。
目前针对KRAS G12C突变的治疗策略正趋向联合用药:JAB-21822正探索与SHP2抑制剂联合,临床实验显示疗效提升,但副反应也相应增加;索托拉西布(Sotorasib)与化疗联合;氟泽雷塞与西妥昔单抗等抗体类药物联合,均观察到疗效改善。
该患者单纯使用靶向治疗未获得显著PFS获益,后续采用免疫治疗联合安罗替尼的方案。此方案选择有其合理性,但在全身治疗(免疫联合抗血管生成治疗)过程中,患者右侧肾上腺病灶逐渐增大,直至疾病进展后才进行局部消融治疗。
对于后续治疗,目前患者仅双侧肾上腺存在病变,且肺部肿瘤切除术后、其他远处部位均控制稳定,应优先考虑局部治疗(如双侧肾上腺根治性放疗)以强化控制;若未来出现多部位进展,可考虑针对肉瘤样癌的化疗方案(紫杉类药物等仍有一定疗效)。
此外,希望听取张旭教授关于双侧肾上腺根治性放疗可行性的意见,并关注患者当前免疫联合安罗替尼治疗副反应逐渐增多的问题,探讨后续治疗调整策略。
张旭教授 这位患者的治疗总体上基本遵循正确路径。发现病情后手术切除病灶,术后纵膈淋巴结阴性、切缘干净(N0分期),当时无需术后放疗。观察到左肾上腺病灶增长时,全身靶向药物治疗可行,但需密切监测局部病灶。后续双侧肾上腺增大,需行局部治疗,患者选择消融治疗。消融相比放疗的优势在于治疗前可通过探针穿刺取病理,明确肾上腺肿物为恶性转移,为治疗提供依据。热消融治疗后,患者局部问题基本解决,胸部手术及双侧肾上腺消融术后,目前体内未见残存实质性肿瘤组织。
当前谈论局部治疗存在难度,因放疗需明确靶区,除非复查证实肾上腺消融不彻底、局部有病灶残存,方可进行放疗。放疗分为体内(粒子植入,持续释放射线,适用于顽固残存病灶,为较靠后选择)和体外治疗,优先选择外照射。放疗时机取决于靶区情况,若PET-CT等检查证实双肾上腺有残存病灶或出现新转移灶,应尽早放疗,避免疾病进展后转为挽救治疗。
放疗与消融作为局部治疗各有优势:消融可术前取病理,但属于有创穿刺治疗,射频或冷冻对周边控制的完善性尚存疑问;放疗局部包绕效果更优,但无法术前获取病理。目前患者仍应以全身治疗为主,密切观察肾上腺局部进展,一旦进展需积极放疗。针对患者双侧肾上腺肿大、仅右侧消融而左侧未治疗的情况,强烈建议对左侧行放疗。
林根教授 从医学角度分析,该患者属于晚期肿瘤,虽已切除肺部肿块,但双肾上腺仍存在转移病灶。因此,治疗原则应以全身综合治疗为主,涵盖免疫治疗、化疗等手段,同时结合局部处理(如消融治疗等)。在疾病未明确进展时,可继续实施全身治疗。值得注意的是,若全身治疗在四个月内即出现进展,可能提示药物已产生耐药性。在此情况下,患者不应过度抵触化疗,因其仍是目前较为适宜的全身治疗方案。化疗可与新一代药物联合使用,例如联合免疫药物(如伊沃西单抗,对免疫耐药患者仍有一定疗效)、双药化疗方案或ADC类药物等。
关于靶向治疗,该患者服用针对KRAS G12C突变的靶向药物后,病情在短时间内出现进展,这也印证了唐俊舫教授的观点,即此类靶向药物对该患者疗效欠佳。因此,全身治疗需先实现有效控制,再考虑局部处理。张旭主任此前提及的射频消融、放疗等局部治疗手段均可作为选择。此外,双肾上腺转移患者中,约30%或更多可能出现肾上腺皮质功能减退,典型症状包括疲乏、无力等,同时机体应激功能也会下降。因此,建议患者检测皮质醇激素水平(包括早、下午及24小时皮质醇定量、ACTH等),以判断皮质功能是否减退。这一情况可能导致患者对治疗的耐受性降低,需与安罗替尼及免疫治疗引起的皮疹、口腔疼痛、鼻出血等副作用加以鉴别,同时还需考虑患者身体耐受情况是否与肾上腺皮质功能减退有关(约30%患者会出现腹泻等症状)。局部治疗(如放疗等)的实施,必须以全身病情得到控制为前提。
针对患者提出的两个问题:其一,目前存在较多适合该患者的临床试验可供选择;其二,从现实情况看,IV期患者实现根治的可能性极低,建议患者做好长期带瘤生存的心理准备。
病例二:多发转移肺腺癌联合治疗方案探讨






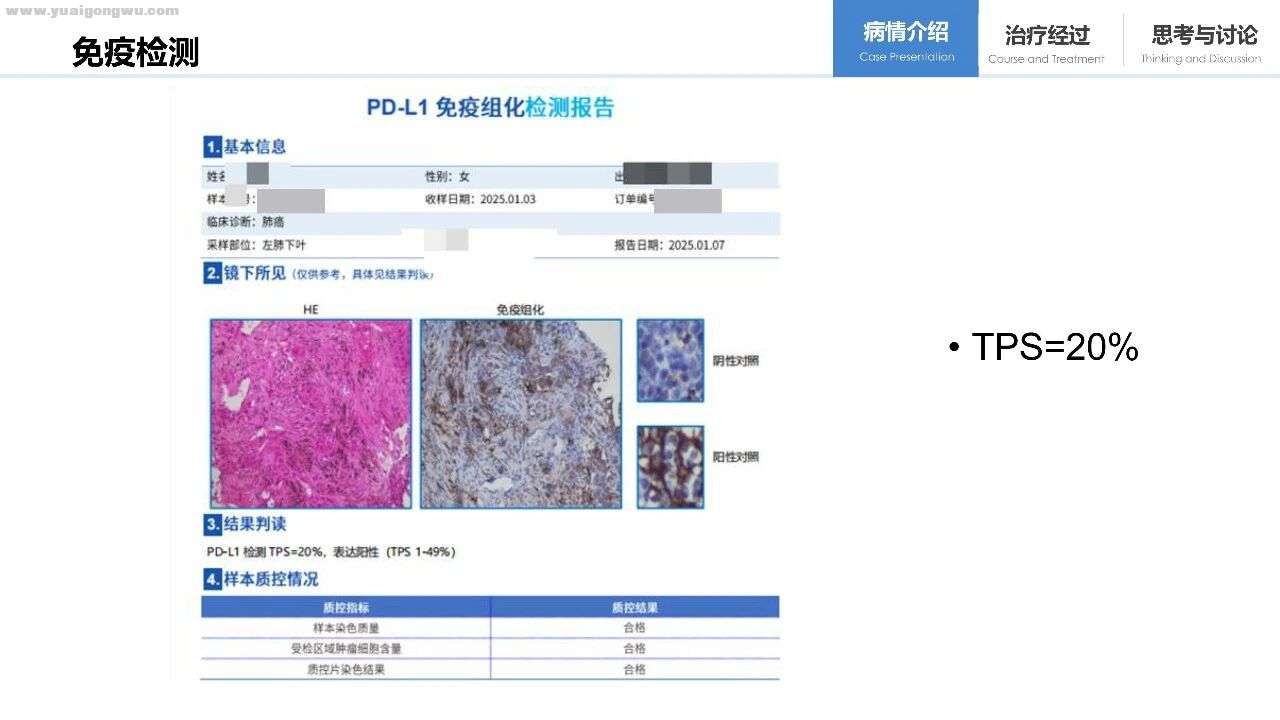



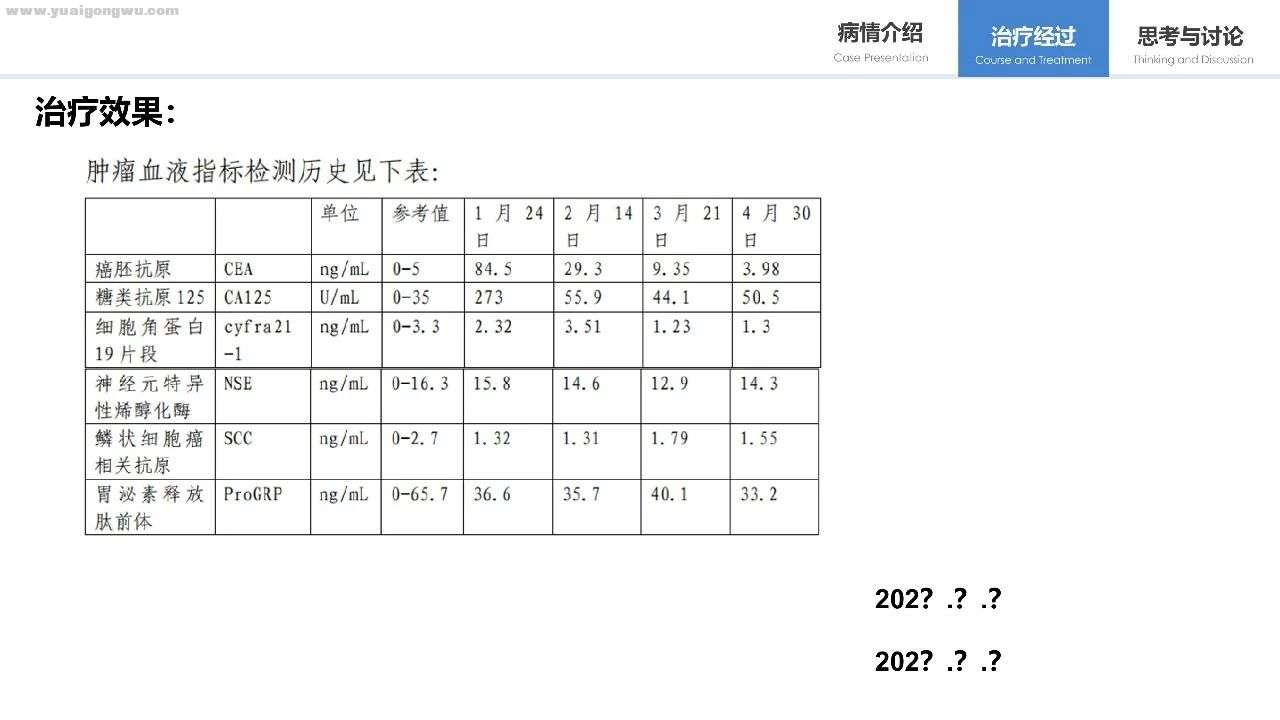








患者诉求: 1、目前脑实质转移控制较好,增强核磁报告未提示脑膜转移,但线上问诊查看头部核磁影像资料有医生提出可能存在脑膜转移。请问:通过影响资料是否认为存在脑膜转移可能?若存在脑膜转移可能,是否需要立即进行脊髓液检测确认并更改治疗方案?
2、现在已进入稳定期,但仅进行了化疗联合靶向治疗。请问:是否需要积极进行放疗(伽马刀、TOMO全脑放疗)或对原发病灶进行介入消融治疗?还是等待药物控制不住发生进展后再进行?如果需要进行更积极治疗建议什么时间开始?
3、在全身控制较好的情况下,增强CT仍提示左侧胸水有缓慢增加,这是什么原因? 需要进行怎样处理?
4、甲状腺低密度结节,在基线检查中未见,但是复查CT中出现,并且进行颈部彩照也反映无异常,是什么原因?需要进行怎样处理?
贺伟教授 患者临床影像表现典型,诊断较为明确。左下肺结节具有典型恶性征象,肺门、纵膈及全身多发淋巴结均存在转移。肺周围可见磨玻璃密度影伴局部网格影,不排除癌性淋巴结转移可能。影像报告显示双肺散在结节,考虑存在双肺转移。脑部核磁提示脑实质多发转移灶,但根据现有脑部影像资料,未见明确脑膜转移征象。若从影像层面确认脑膜转移,需核磁报告提供全面多序列影像以辅助判断。
关于患者甲状腺结节问题,其基线检查未见异常,首次复查CT报告显示7毫米甲状腺结节(因描述欠清晰,无法确定为增强CT或平扫检查)。后续检查结果显示,2025年2月至4月期间结节影像无明显变化,结合彩超结果的描述,考虑良性病变可能性较大。建议患者后续至正规医疗机构定期进行甲状腺B超复查。
杨志教授 对于明确存在多发转移的晚期肺腺癌患者,从外科角度而言,已无显著干预指征。患者基因检测显示EGFR19外显子敏感突变,采用化疗联合靶向治疗方案,目前疗效尚可。针对患者多发脑转移的情况,个人建议可尝试将某些靶向药物双倍剂量使用,以观察对脑转移病灶的控制效果是否更佳。当然,此方案需内科专家进行专业评估,上述观点仅供参考。
唐俊舫教授 第一个问题是患者是否存在脑膜转移。对于存在EGFR突变的患者,在靶向治疗过程中通常高度重视颅内病变的控制,尤其是对是否会出现脑膜转移的情况较为关注。该患者最初确诊时伴有轻微厌食、呕吐症状,通过靶向联合化疗后这些症状得到缓解,而这些症状可能与脑膜转移有关,也可能与脑实质转移病灶存在一定相关性。至少从目前影像来看,无法确定存在明确的脑膜转移。若要确定是否存在脑膜转移,一方面需通过增强脑核磁的定期复查来仔细判断是否有脑膜转移的典型影像,另一方面若怀疑出现脑膜转移,可进行腰穿及脑脊液化验来进一步明确可能性。
在患者治疗方面,其选择FLAURA2模式是较为合理的选择。作为肿瘤负荷较大、伴有脑转移的EGFR19缺失突变且带有TP53突变的患者,在身体耐受的情况下选择该模式较为恰当。且患者的治疗过程规范,一线采用奥希替尼联合培美曲赛加卡铂方案进行四个周期治疗后,以奥希替尼和培美曲赛单药维持治疗,这属于标准的FLAURA2模式,目前该方案对全身肿瘤的控制较为稳定。
关于患者的胸腔积液问题,其最初诊断时就存在少量胸腔积液,因量少无法进行诊断性穿刺,治疗过程中观察到积液量稍有增加但基本稳定。对于单侧胸腔积液需高度警惕是否存在胸膜转移可能,这需要定期观察胸水的量的增长情况,必要时进行诊断性穿刺以进一步明确胸水性质,还可考虑进行PET-CT检查,查看胸膜位置是否有高代谢提示。若经检查发现胸水增加且存在胸膜转移,可考虑在FLAURA2模式基础上加用安罗替尼等多靶点抗血管药物,这种联合治疗可能对胸膜转移及胸腔积液的控制有帮助。
针对患者的脑实质转移情况,通过对比其脑核磁影像可知,经靶向治疗后目前控制良好,针对脑部病变进行伽马刀等局部治疗目前必要性不大,建议定期复查脑核磁,若脑部出现进展,可考虑进行局部伽马刀治疗。而对于患者的甲状腺结节问题,在复查过程中可见七毫米的结节无变化,建议定期进行超声复查。
张旭教授 该患者为肺腺癌Ⅳ期全身多发转移,初始治疗前病情较重,经靶向联合化疗及抗骨转移骨保护剂治疗后,病情得到良好控制。就患者相关问题分析如下:
头部病变经前后核磁影像对比,多个病灶治疗后均呈好转趋势。脑膜转移虽难以确切确认,但即便存在,目前大概率也在好转。确认脑膜转移需在影像或体感有明显证据时,再行脑脊液检测,不建议非必要情况下单独进行该项检测。
奥希替尼对中枢神经病灶控制效果较好,当前脑部处于稳定期,暂无需急于采用伽马刀局部处理或TOMO全脑放疗,可继续观察。伽马刀与TOMO的区别在于,前者适合局部小病灶的点对点精准处理,疗效显著;后者照射野大,不受靶区范围限制,可实施全脑或全脑全脊髓放疗,具体选择需依据病情需求。肺部原发灶若考虑放疗,需把握治疗后病灶不再继续缩小的时机,处于稳定期时是否选择放疗需谨慎考量。对肺部原发灶进行局部干预时,放疗与消融均为可考虑的方案,具体需由医生评估,选择风险更小的方式。
全身病情控制下,左侧胸水呈缓慢增加态势,经仔细阅片发现,其增加程度极为有限,量处于少量或极少量水平,可密切观察。若胸水进一步增多,可抽取胸水以明确性质,为后续治疗提供依据。关于甲状腺结节,考虑可能是基线检查时存在遗漏未报,后续复查显示其一直稳定在7毫米。鉴于肺癌通常较少转移至甲状腺,相对全身其他问题,该结节问题不大,定期复查即可。
综上,患者目前治疗后病情稳定,以定期复查为主,若出现局部寡进展或原发病灶寡残存,可积极考虑局部治疗。
林根教授 患者选择靶向联合化疗的方案是合理的。由于患者存在全身多发转移且病灶负荷较大,同时基因检测显示合并TP53突变与MYC扩增,这类突变患者的靶向药物易出现耐药,药物控制时间相对较短。此外,同时合并这两个基因的患者在定期随访时需特别留意,部分患者可能会出现病理向小细胞肺癌转化的情况(MYC扩增、RB1基因突变等均可能引发小细胞转化)。MYC扩增作为恶性程度较高的癌基因,会驱动肿瘤的恶性生物学行为,因此当前治疗方法正确。
第二点,患者无需过度焦虑。绝大多数肿瘤患者在治疗有效后会进入稳定的平台期,且在稳定一段时间后才可能出现耐药,这是疾病变化的基本规律。在疾病处于平台期或肿瘤缩小趋势中,体内肿瘤大小可能会有一定波动,因此对于少量胸水增加或肿瘤略微进展的情况,不必过于紧张。而且,判断肿瘤是否进展有明确标准,患者无需为此焦虑。
第三点,一个人可能同时患有多种疾病,除肿瘤外还可能有其他病症。患者的甲状腺结节可能是甲状腺癌、甲状腺腺瘤,也可能是免疫性甲状腺疾病。但无论属于哪种情况,通常都不会影响当前肺癌的治疗进程。即便为甲状腺癌,其通常也是惰性肿瘤,治疗仍以当前肺癌治疗为主。
关于是否存在脑膜转移,由于提供的片子较少,需以现场查看磁共振片子为准。从患者提供的部分脑核磁影像来看,脑部转移灶多靠近脑实质表面,这类转移病灶可能容易导致肿瘤细胞脱落进入脑脊液从而形成脑膜转移。因此,患者在治疗过程中需密切关注身体症状变化,建议找有经验的医生对当前核磁影像片子进行审核。
病例三:三代EGFR-TKI耐药后的策略优化











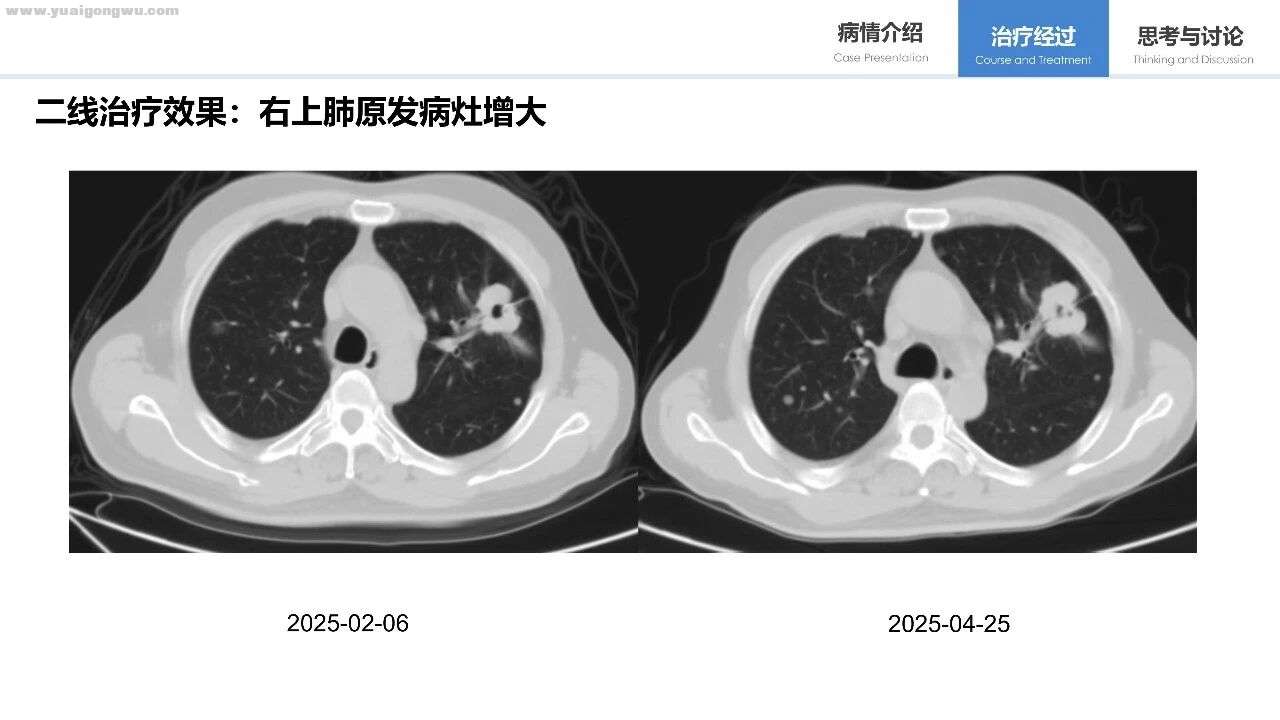


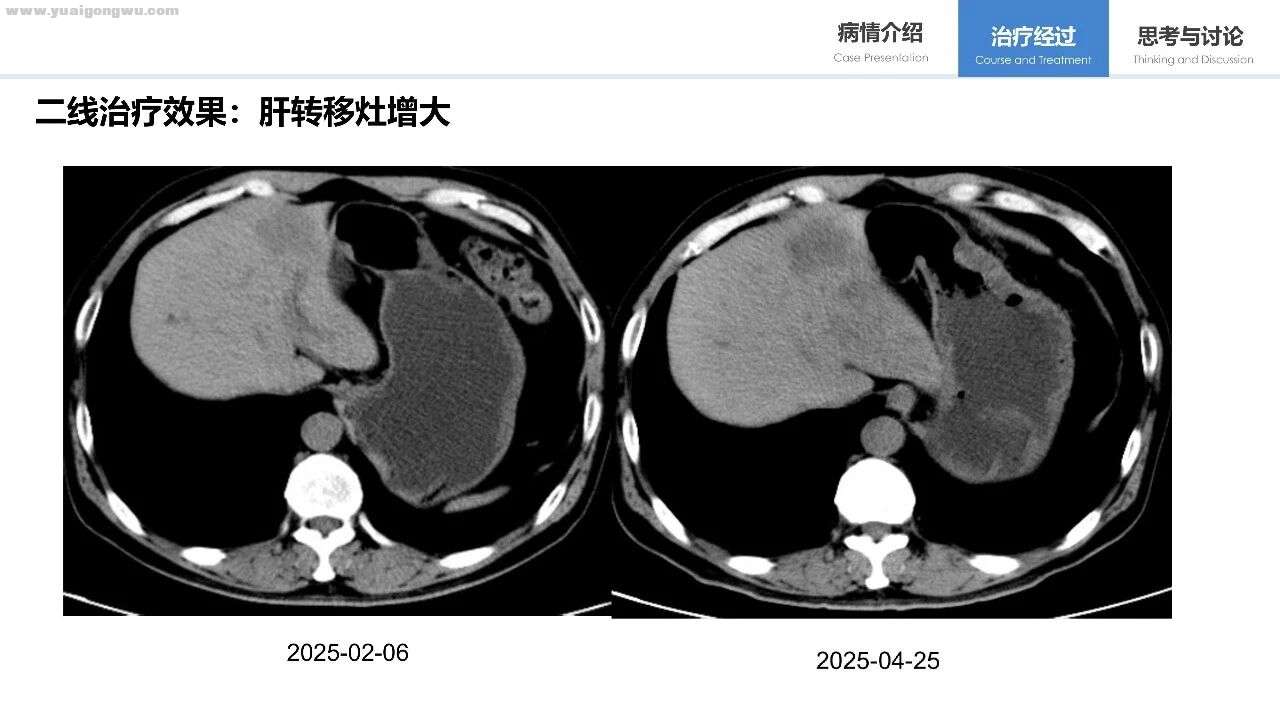



患者诉求: 1、EGFR敏感突变晚期肺癌患者一线治疗方案如何选择?
2、二线阿美替尼+培美曲塞+卡铂+贝伐珠单抗2周期进展,三线方案怎样选择?
3、使用依沃西单抗期间阿美替尼是否继续应用?
4、如果三线治疗进展,是否建议再次活检、再次基因检测?后续有哪些治疗方案?
杨志教授 这是个晚期病人,从外科角度而言,已无干预指征,目前治疗具有合理性。
张旭教授 该患者的治疗总体较为合理。患者存在EGFR敏感突变,选择阿美替尼联合贝伐珠单抗的方案并无不妥,且在治疗过程中,对脑转移灶及髂骨转移灶及时采取了积极的放疗措施,值得肯定。其一线治疗无进展生存期(PFS)为10个月,在靶向突变患者中属于平均水平,疗效尚可。
关于二线及三线治疗,内科医生可给出更优化的建议。若三线治疗出现疾病进展,个人建议:在全身治疗的基础上,选择合适且有效的系统治疗方案,同时针对局部靶病灶采用短疗程、低损伤的放疗模式,如8Gy×3次等。考虑到患者为EGFR突变且已出现耐药,此前也应用了依沃西单抗,若在免疫治疗介入时联合放疗,可斟酌作为一种治疗选择。但需注意,放疗剂量不宜过大,疗程不宜过长,以短频快的方式进行局部姑息减症治疗,避免增加患者不良反应,这是放疗可参与的治疗方向。
唐俊舫教授 对于肿瘤负荷大、病期晚且存在 EGFR 敏感突变的晚期肺腺癌患者,一线治疗优先选择三代TKI。当合并共突变、肿瘤负荷大或脑转移时,联合治疗方案的选择尤为关键。前一病例采用FLAURA2 模式(三代TKI联合化疗)可延长无进展生存期(PFS),而该患者一线选择三代TKI联合贝伐珠单抗,考虑到其严重脑水肿,贝伐珠单抗对减轻脑水肿有明确作用,这一选择具有合理性。
该患者一线PFS约10个月,疗效不甚理想,可能与肿瘤负荷大及合并共突变相关。一线治疗后出现缓慢进展,尝试靶向药加量使PFS进一步延长,后续联合化疗期间,双肺转移病灶经两次影像对比显示有相对快速进展,随即换用依沃西单抗(PD-1/VEGF双特异性抗体)联合培美曲赛、卡铂的化疗方案,这属于EGFR-TKI进展后的标准治疗方案。在此需探讨阿美替尼是否需持续应用,因既往临床研究显示EGFR-TKI与免疫PD-1单抗联合时不良反应可能增加,该问题有待进一步探讨。
患者一线治疗后再次活检发现PTEN等新突变,目前缺乏对应的靶向药物。鉴于患者三线治疗仅完成两个周期,尚未复查评估疗效,若治疗有效可按原方案继续;若病情进展,建议再次活检以明确是否存在可靶向治疗的耐药靶点,若仍无合适靶点,三线治疗可考虑TROP2 ADC类药物(如芦康沙妥珠单抗,其与多西他赛对比的临床研究显示可显著延长PFS),或埃万妥单抗联合化疗等方案。
林根教授 若患者当前仍在接受相关治疗,务必立即停用阿美替尼。其依据在于,既往研究表明靶向治疗与免疫治疗联合使用时,患者间质性肺炎等严重不良反应的发生率会显著升高。尽管不同靶向药物与免疫药物联合使用的反应尚未完全明确,但鉴于阿美替尼已丧失疗效,继续与依沃西单抗联合,不仅无法达到治疗效果,还极有可能引发严重不良反应,这一建议至关重要,希望患者能够重视,对于无效的药物必须果断停用。
该患者在治疗过程中持续使用靶向药物,而培美曲塞联合卡铂的化疗方案在短期内使用后,就观察到肿瘤快速进展。虽然目前尚无法确定培美曲塞联合卡铂与免疫治疗能否产生协同效应,但倘若后续病情仍继续进展,则需要更换治疗方案。例如,可选用二线化疗药物,如此前未使用过的紫杉烷类单药,同时联合安罗替尼(鉴于贝伐珠单抗使用后,安罗替尼仍可能有效)。此外,唐俊舫教授提及的TROP2 ADC类药物芦康沙妥珠单抗,以及埃万妥单抗联合化疗等多种方案均可作为备选。
从整个治疗过程可以看出,在治疗中必须严格把控疗效与风险,许多传统治疗习惯可能需要调整。目前已知HER2扩增可能是导致耐药的原因之一,因此强烈建议患者在三线治疗后再次进行活检和基因检测,这将为后续寻找合适的治疗方案提供重要依据。
结束语
在直播活动最后,林根教授总结道:作为医生,职业操守与满足感往往源于病人的鼓励和支持,病人在治疗过程中的肯定,是医生不断前行的动力。以今天三个病例的准备工作为例,各位医生聚在一起,花费大量时间共同研讨,这正体现了医患双方在面对肿瘤这一共同敌人时,同心同德与之抗争的决心。希望此类活动能够长期坚持下去,切实为患者提供帮助。尽管每月全国仅征集三个病例,力量有限,但这传递出一个重要理念:多学科诊疗(MDT)至关重要,各学科既有自身优势,也存在相对薄弱之处,而通过学科间的紧密配合,就能像齿轮一样精准咬合,为患者提供最适宜的诊疗方案。
首都医科大学附属北京胸科医院 患者门诊申请肿瘤多学科诊疗(MDT)流程
1 服务对象 自愿申请或门诊出诊医生认为有必要行肿瘤多学科诊疗的患者。 2 服务时间 每周三下午15时至16时 3 服务收费 依据当日肿瘤MDT排班医生级别收费 4 服务要求 由当日肿瘤MDT主席给予患者及家属诊疗结论。
具体执行流程
1 患者于当日上午肿瘤门诊就诊(各级别均可,建议挂肿瘤科普通号即可) 2 由出诊医师审核患者携带资料是否完整,是否可供MDT专家进行讨论研判。资料不完整者予以告知患者待资料完善后再行就诊。 3 资料完整、需求合理的患者可由出诊医生协助患者完成当日MDT专家号预约(依据当日我院MDT排班专家职称予以挂号)。 4 患者缴费挂号后请出诊医师书写MDT会诊申请单,让患者或者家属于下午会诊时交给当日MDT秘书。 5 告知患者当日下午14时于我院手术室二楼家属等候区等待,将完整资料和会诊单交给当日MDT秘书。 6 经MDT讨论后由MDT秘书将结论书写于会诊单上并由当日MDT主席向患者或其家属解释诊疗结论。
|